Contoh Soal Penyetaraan Reaksi Homecare24

Cara Mudah Menyetarakan Persamaan Reaksi Kimia Part 2 вђ Tips And Solution Untuk memperdalam pemahamanmu tentang penyetaraan reaksi redoks, berikut ini adalah beberapa contoh soal yang dapat kamu gunakan sebagai latihan: apa itu reaksi oksidasi reduksi? reaksi oksidasi reduksi atau yang biasa disingkat dengan reaksi redoks adalah suatu reaksi kimia yang melibatkan transfer elektron antara dua unsur atau molekul. Dengan melakukan penyetaraan reaksi redoks dengan metode biloks reaksi, maka kamu dapat memastikan bahwa reaksi kimia benar benar seimbang dan memenuhi kriteria aturan konservasi massa dan energi. jika kamu ingin belajar lebih lanjut tentang reaksi kimia dan membuat persamaan reaksi kimia, kamu dapat terus mengasah kemampuanmu dengan berbagai.
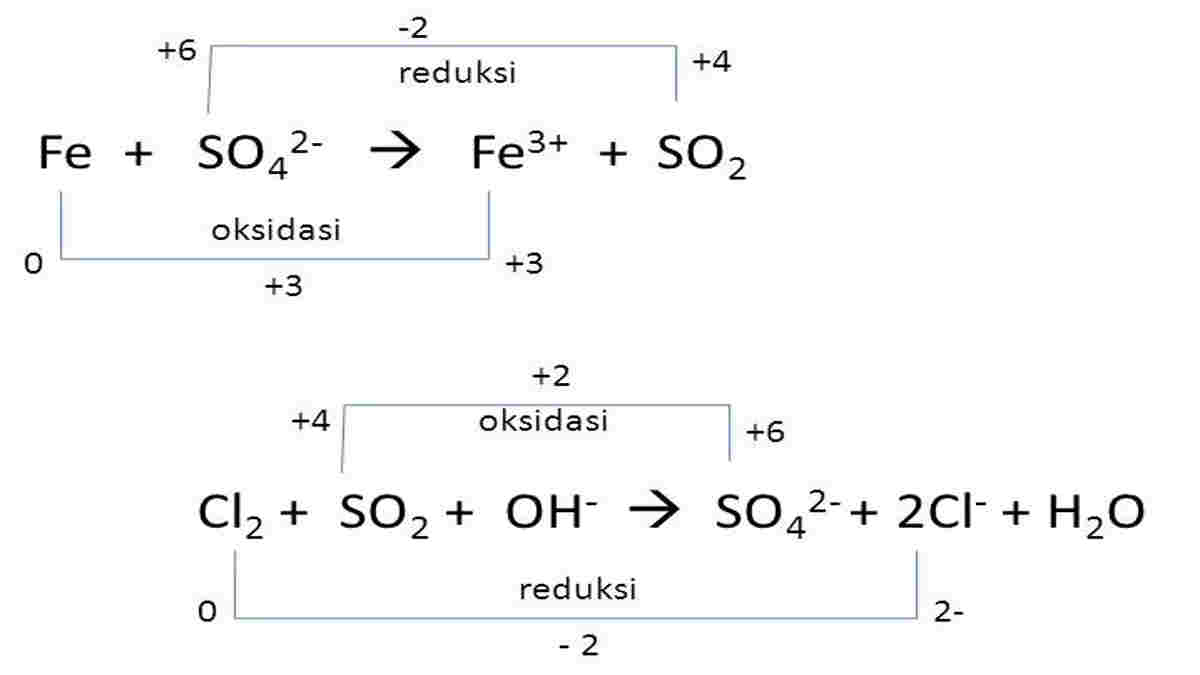
Persamaan Reaksi Pengertian Penyetaraan Dan Contoh So Vrogue Co Penyetaraan reaksi redoks metode setengah reaksi adalah salah satu metode penyetaraan reaksi redoks. dalam metode ini, reaksi yang terjadi dipisahkan menjadi dua setengah reaksi yaitu reaksi oksidasi dan reaksi reduksi. setiap setengah reaksi kemudian diimbangi dengan menambahkan kofaktor yang sesuai agar jumlah elektron yang terlibat dalam. Supaya lebih jelas dan paham, perhatikan beberapa contoh berikut ini. contoh soal #1. tuliskan dan setarakan persamaan reaksi antara gas metana (ch4) dengan gas oksiden membentuk gas karbon dioksida dan uap air. jawab: langkah 1, menuliskan rumus kimia dan persamaan reaksi. Pembahasan. kita dapat menyelesaikan soal tersebut dengan menggunakan metode penyetaraan reaksi kimia. langkah langkahnya adalah sebagai berikut: 1. tuliskan reaksi kimia yang diberikan. 2. tentukan unsur mana yang belum seimbang pada reaksi tersebut. pada reaksi di atas, unsur yang belum seimbang adalah hidrogen (h). 3. Reaksi yang mengikat oksigen. yang melepaskan electron. reaksi yang mengalami kenaikan bilangan oksidasi. bertindak sebagai reduktor. jadi, reaksi oksidasi terdapat pada nomor 1 ditandai dengan adanya pengikatan oksigen dan 4 ditandai dengan adanya kenaikan biloks dari 5 menjadi 7.

Comments are closed.